Covid-19: Le vaccin AstraZeneca peut-il changer la donne dans la stratégie vaccinale française?
CORONAVIRUS - Premier commandé, dernier injecté? Ce lundi 4 janvier, le vaccin contre le Covid-19 mis au point par le laboratoire AstraZeneca et l’université d’Oxford a été utilisé pour la première fois au Royaume-Uni. Un “tournant” dans la...
REJOINDRE L'ÉQUIPE DE RÉDACTION
Tu penses avoir un don pour la rédaction ?
Contacte-nous dès maintenant pour rejoindre notre équipe de bénévoles.
REJOINDRE L'ÉQUIPE DE RÉDACTION
Tu penses avoir un don pour la rédaction ?
Contacte-nous dès maintenant pour rejoindre notre équipe de bénévoles.
REJOINDRE L'ÉQUIPE DE RÉDACTION
Tu penses avoir un don pour la rédaction ?
Contacte-nous dès maintenant pour rejoindre notre équipe de bénévoles.
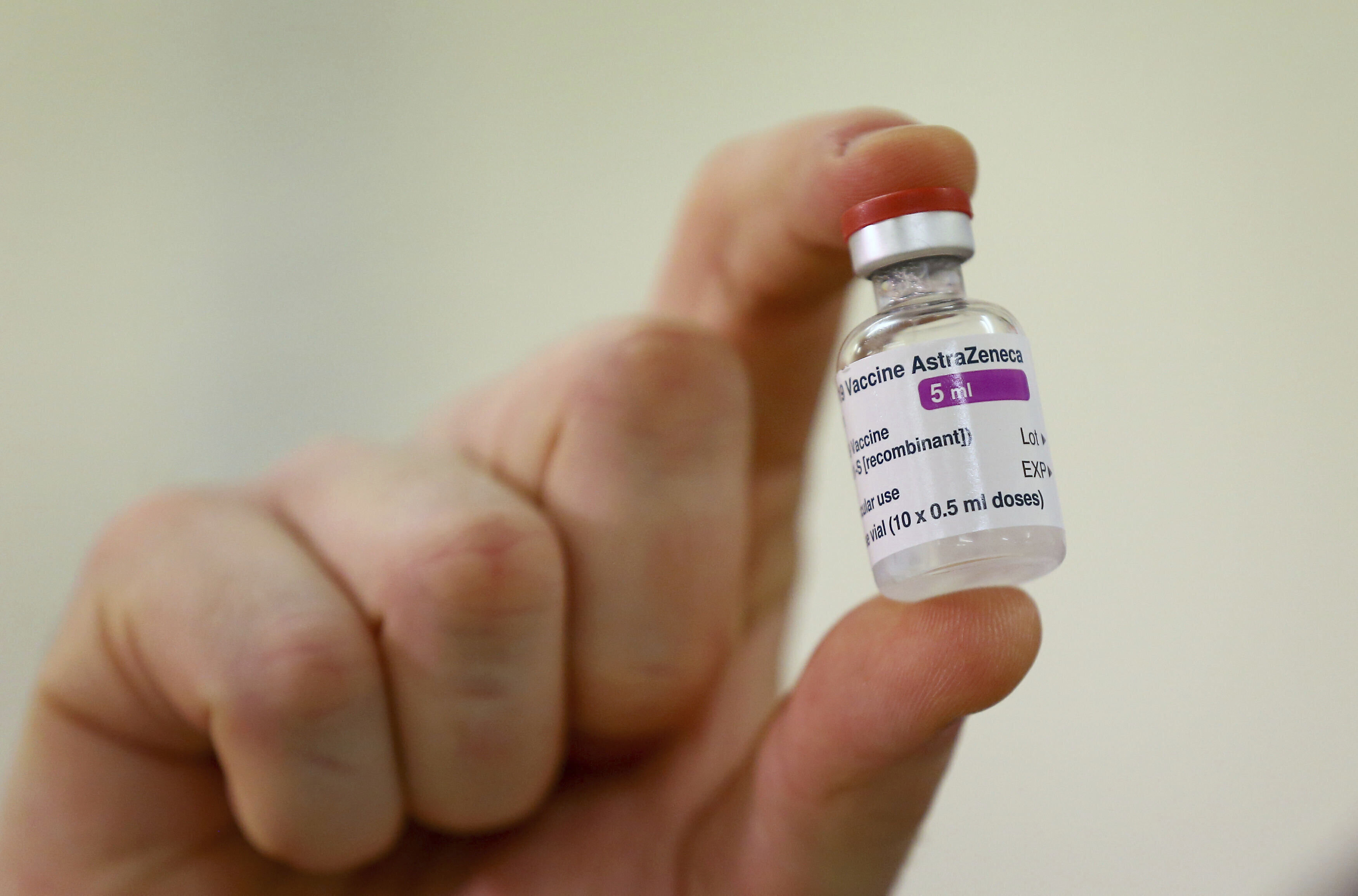
CORONAVIRUS - Premier commandé, dernier injecté? Ce lundi 4 janvier, le vaccin contre le Covid-19 mis au point par le laboratoire AstraZeneca et l’université d’Oxford a été utilisé pour la première fois au Royaume-Uni. Un “tournant” dans la lutte contre le virus pour le gouvernement britannique qui pourrait aussi être bienvenu en France, où les critiques sur la stratégie vaccinale se multiplient en pleine seconde vague qui s’éternise.
Un an après le début de la pandémie, un nouveau vaccin est désormais sur le marché: celui d’AstraZeneca sur lequel le Royaume-Uni, l’Argentine et l’Inde misent pour accroître leur taux de vaccination. Ils ne sont pas les seuls: dès le mois de juin 2020, quatre pays européens ont passé leurs toutes premières précommandes auprès du groupe pharmaceutique. Y compris la France.
Six mois plus tard, c’est pourtant un autre produit qui occupe le devant de la scène nationale: le vaccin de Pfizer/BioNTech - le seul administré dans l’Hexagone à ce jour.
Après des débuts prometteurs, le vaccin d’AstraZeneca s’est donc fait voler la vedette. Mais alors que la polémique monte sur les “lenteurs” de la campagne de vaccination, ce vaccin et ses spécificités pourraient s’inviter à la “réunion de travail et de suivi sur les vaccins” qui devait se dérouler ce lundi après-midi à l’Élysée autour d’Emmanuel Macron.
Un vaccin plus solide pour aller plus vite?
L’arrivée du vaccin Pfizer/BioNTech, le premier utilisé sur le territoire national, a été applaudie avant les fêtes. Mais depuis, les Français ont déchanté: avec 500 personnes vaccinées en une semaine, contre plus de 200.000 en Allemagne, les espoirs d’une sortie rapide de la crise sanitaire ont été douchés.
Contraints de se justifier, les membres du gouvernement ont réfuté toute lenteur de la stratégie française. Tour à tour, ils ont évoqué plusieurs raisons comme le laps de temps nécessaire pour identifier les volontaires (notamment dans les Ehpad) mais aussi les questions de “logistique” posées par le vaccin Pfizer/BioNTech en termes de transport et de stockage.
Une argumentation valable au moins sur le dernier point: des trois vaccins particulièrement attendus en Europe, celui de Pfizer est l’un des plus fragiles. Difficile à transporter, sa durée de vie dans un réfrigérateur traditionnel entre 2 et 8°C ne dépasse pas 5 jours, et même si des super-congélateurs ont été commandés pour en faciliter la gestion, ces contraintes ralentissent forcément la distribution: des vaccins difficiles à conserver compliquent une stratégie de vaccination rapide sur une large échelle.
Cet écueil - que l’on retrouve chez le vaccin Moderna- est en partie réglé avec AstraZeneca. À la différence de ses concurrents, le vaccin du groupe britannique peut être conservé à long terme entre 2 et 8°. Les pharmacies, centres hospitaliers et Ehpad peuvent donc plus facilement emmagasiner les doses, pendant une durée plus longue. Et à long terme, vacciner davantage de personnes dans des délais plus courts.
Un vaccin efficace... mais sur qui?
Le vaccin AstraZeneca/Oxford est un vaccin ”à vecteur viral”: il prend comme support un autre virus (un adénovirus de chimpanzé) qui a été transformé et adapté pour combattre le Covid-19. La manière qu’il a de délivrer du matériel génétique dans les cellules, leur ordonnant d’attaquer le SARS-CoV-2, a été présenté comme un “cheval de Troie”.
Ses débuts ont cependant été difficiles: après avoir annoncé une efficacité de 70% en moyenne face à des concurrents autour de 90%, il a dû passer fin novembre des tests supplémentaires pour répondre à des critiques sur la méthodologie des essais cliniques.
Au final, le résultat est probant: le 27 décembre, le directeur général d’AstraZeneca Pascal Soriot a assuré que le laboratoire pensait avoir trouvé “la formule gagnante et comment arriver à une efficacité qui, avec deux doses, est élevée comme celle des autres” avec une “protection de 100%” contre les formes sévères du Covid-19. Selon AstraZeneca, le vaccin est également capable de combattre le nouveau variant du coronavirus, même si des essais doivent encore être menés pour confirmer cette hypothèse.
Dans une France où le gouvernement s’est fixé comme objectif de vacciner un million de personnes avant fin février, ces résultats, couplés à une logistique simplifiée, ont de quoi séduire. Pourtant, le vaccin AstraZeneca pourrait bien ne pas tout à fait répondre à la stratégie vaccinale française.
Pas de données, pas (encore) de feu vert
À ce jour, le vaccin AstraZeneca est le seul à avoir eu des résultats validés par une revue scientifique. Dans un avis rendu public le 8 décembre, les scientifiques de The Lancet le considèrent comme “sûr” et confirment son efficacité à 70%.
Mais ils soulignent aussi un gros point négatif: les essais d’AstraZeneca n’ont que peu porté sur les populations les plus exposées aux formes graves de la maladie, à savoir les plus de 65 ans. Seulement 12,1% des patients passés par les essais cliniques avaient plus de 55 ans, rappelle le groupe de scientifiques. Leur conclusion: “nous ne pouvons pas encore déduire l’efficacité chez les adultes plus âgés, qui sont le groupe le plus à risque de résultats sévères du COVID-19.”
Ce détail pourrait freiner les impatiences françaises: le gouvernement ayant choisi de proposer en priorité la vaccination aux personnages de plus de 65 ans vivant et travaillant dans les établissements de santé, l’efficacité du vaccin sur cette tranche de population est essentielle. “Il faut garder son calme et garder les priorités, parce que si on vaccine beaucoup mais pas les bons, on va mettre des mois à diminuer les hospitalisations et les décès”, a d’ailleurs déclaré sur RMC/BFMTV la présidente de la HAS, Dominique Le Guludec, en défendant le rythme français.
De même, l’Agence européenne du Médicament a aussi exigé de disposer de davantage de données avant de se prononcer. Son avis est décisif: ce n’est qu’une fois validé par l’AEM que le vaccin serait soumis à la Commission européenne, avant un dernier accord délivré par les autorités nationales - la Haute Autorité de santé en France.
Dans son ensemble, le processus de validation pour une mise sur le marché peut prendre plusieurs semaines. Et il n’est pas près de commencer: le 31 décembre, l’Agence européenne du médicament estimait peu probable une autorisation de mise sur le marché en janvier.
À voir également sur Le HuffPost: Covid-19: le Royaume-Uni commence à injecter le vaccin AstraZeneca-Oxford